Có thể bù đắp khiếm khuyết gen bằng vitamin và khoáng chất
Trong vòng 5 năm nữa chi phí thiết lập trình tự gen người sẽ giảm nhanh chóng, dự đoán mức giá khoảng 100 đô la cho một người. Chẳng mấy chốc lý do duy nhất khiến bạn không muốn xem “bản đồ gen” cá nhân đó là sợ nhìn thấy những khiếm khuyết trong hệ gen của mình.
Tuy nhiên các nhà khoa học thuộc đại học California Berkeley lại đưa ra một nguyên nhân tích cực khuyến khích tìm hiểu về vốn gen di truyền của mỗi chúng ta nhằm tìm kiếm khiếm khuyết di truyền nhỏ có thể khôi phục nhờ các biện pháp đơn giản với vitamin hoặc khoáng chất.
Giáo sư sinh học tế bào và phân tử Jasper Rine (Đại học California Berkeley) cho biết: “Tôi đang tìm kiếm những thông tin tích cực trong hệ gen của con người”.
“Báo chí trong suốt 20 năm qua liên tục nói về thành công trong lĩnh vực nghiên cứu y sinh học nhằm tìm kiếm gen gây bệnh có sức lôi cuốn về mặt sinh học, có tầm quan trọng lớn về mặt di truyền đối với những người tiếp nhận thông tin. Tôi bị ám ảnh với công việc tìm kiếm nhóm thông tin di truyền khác khuyến khích con người tiến hành phân tích hệ gen của họ”. Những gì ông và cộng sự của mình phát hiện đã được trình bày trên số ra trực tuyến của tờ Proceedings of the National Academy of Sciences (PNAS). Trong bài có viết khác biệt di truyền lớn khiến enzim của người kém hiệu quả hơn bình thường, nguồn bổ sung vitamin có thể khôi phục các enzim khiếm khuyết để trở lại họat động với hiệu quả tối đa.
Nhà khoa học Nicholas Marini (đại học California Berkeley) đồng thời là tác giả đầu tiên của bài viết nhấn mạnh rằng bác sĩ thường kê đơn thuốc với vitamin nhằm chữa nhiều hiện tượng khiếm khuyết trao đổi chất hiếm gặp, có khả năng gây chết người gây ra bởi một số enzim quan trọng bị đột biến. Những người phải chịu đựng các bệnh về trao đổi chất chính là những người phải nhận hai bản sao “kém chất lượng” (hay hai alen) của một enzim chủ chốt. Nhiều người khác chỉ nhận 1 gen xấu hoặc hai bản sao của gen lỗi nhẹ nhưng vẫn làm giảm tỉ lệ enzim gây ra những hậu quả khó thấy mặc dù vẫn có thể điều trị nhờ bổ sung vitamin.
Marini cho biết: “Nghiên cứu đã thuyết phục chúng tôi rằng có rất nhiều biến thể enzim trong quần thể dân cư, rất nhiều biến thể trong số đó gây ảnh hưởng đến chức năng của enzim và cũng rất nhiều biến thể có phản ứng với vitamin. Tôi không hề ngạc nhiên nếu ai đó đòi hỏi liều vitamin tối ưu tùy thuộc theo vốn gen của họ, dựa trên loại biến thể enzim phụ thuộc vitamin mà họ đang mang trong người”.
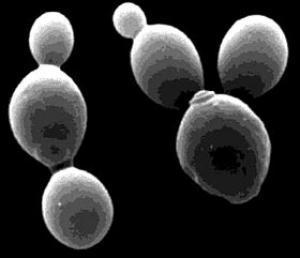 |
Ảnh hiển vi điện tử men Saccharomyces cerevisiae đang sinh sôi. Các nhà nghiên cứu thuộc đại học California Berkeley đã đưa rất nhiều enzim của người vào men để xem liệu những enzim này có thể hoà hợp với vitamin hay không. (Ảnh: Đại học California Berkeley) |
Mặc dù nghiên cứu ban đầu tiến hành thử nghiệm chức năng biến thể gen người bằng cách cấy ghép vào tế bào men nơi mà chức năng của chúng được đánh giá chính xác, Rine và Marini tự tin rằng kết quả vẫn đúng với cơ thể người. Nghiên cứu của họ một phần được Cơ quan phòng vệ dự án nghiên cứu tiến bộ (DARPA) và quân đội Hoa Kì tài trợ. Nghiên cứu giúp họ tạo điều kiện cho nhóm thử nghiệm giả thuyết của mình trên những người lính rằng bổ sung vitamin có thể khôi phục enzim khiếm khuyết. Rine nói: “Các quân nhân của chúng tôi, giống như các vận động viên hàng đầu, phải hoạt động trong môi trường cực kì khắc nghiệt tuy nhiên chức năng sinh lý của cơ thể có thể hạn chế khả năng của họ. Hiện chúng tôi đang phối hợp với cơ quan phòng vệ nhằm nhận diện biến thể enzim có thể khôi phục với hy vọng phát hiện biến thể tồn tại trong quân đội, đồng thời tiến hành thử nghiệm liệu việc bổ sung thích hợp có thể tăng cường hoạt động cho quân nhân hay không”.
Trên tờ PNAS, Rine, Marini cùng đồng nghiệp đã công bố phân tích đầu tiên của họ về biến thể enzim ở người có tên methylenetetrahydrofolate reductase (MTHFR). Enzim này cần phải có vitamin B để hoạt động bình thường, nó giữ vai trò chủ chốt trong quá trình tổng hợp phân tử tạo thành khối nucleotit của ADN. Một số dược phẩm ung thư, như methotrexate, hướng mục tiêu đến MTHFR nhằm ức chế tổng hợp ADN, ngăn ngừa khối u phát triển.
Với nguồn ADN mẫu của 564 người tham gia thuộc nhiều chủng tộc, nhóm dân cư khác nhau, nhóm nghiên cứu tại Cơ quan hệ thống sinh học ứng dụng (thành phố Foster, Calif) đã tiến hành thiết lập trình tự 2 alen mã hóa enzim MTHFR ở mỗi người. Tương ứng với các nghiên cứu trước đó, họ phát hiện 3 biến thể phổ biến của enzim nói trên, kèm theo 11 biến thể hiếm gặp với tỉ lệ dưới 1% mỗi biến thể trong mẫu.
Sau đó họ tổng hợp gen cho mỗi biến thể enzim. Marini, Rine và các cộng sự thuộc trường đại học California Berkeley của họ sau đó đưa những gen này vào tế bào men riêng biệt nhằm kiểm định hoạt động của mỗi biến thể. Men sử dụng nhiều biến thể của cùng một enzim cùng với cơ chất vitamin và khoáng chất giống như con người. Theo Rine, men chính là mô hình lý tưởng để nghiên cứu hoạt động trao đổi chất ở người.
Họ nhận thấy 4 loại đột biến khác nhau ảnh hưởng đến chức năng enzim của người trong men. Một trong những đột biến nói trên rất phổ biến: gần 30% dân số có một alen, khoảng 9% dân số có 2 alen. Bổ sung vitamin B folate vào môi trường nuôi cấy men để phục hồi toàn bộ chức năng cho tất cả các biến thể phổ biến nhất chỉ trừ những biến thể hiếm gặp.
Trong quá trình thí nghiệm, thêm 30 biến thể enzim MTHFR khác được phát hiện, và thử nghiệm 15 trong số đó. “Hơn một nửa rối loạn chức năng enzim, hình thành nên số lượng họat động enzim lớn gấp trăm lần. Đa phần trong số chúng có thể được khôi phục một phần hoặc hoàn toàn nhờ folate (axit folic). Đúng là điều đáng ngạc nhiên”.
Phần lớn các nhà khoa học nghĩ rằng đột biến có hại sẽ bị tiến hóa đào thải, nhưng Rine chỉ ra rằng điều này chỉ đúng với đột biến ảnh hưởng đến khả năng sinh sản. Đột biến tác động đến sức khỏe về sau không bị tiến hóa loại bỏ mà vẫn tồn tại trong hệ gen của chúng ta mãi mãi.
Tác động đối với sức khỏe của việc khôi phục chức năng enzim ở con người vẫn chưa được nắm rõ, tuy nhiên folate - đã được biết đến với khả năng phòng ngừa khiếm khuyết bẩm sinh - dường như còn có thể ngăn ngừa bệnh tim và cả ung thư nữa. Một khiếm khuyết trên enzim MTHFR thúc đẩy sản xuất homocysteine chuyển hóa trong máu với tỉ lệ cao làm tăng nguy cơ mắc bệnh tim và đột quỵ - những căn bệnh thường xảy ra với những người đã qua độ tuổi sinh sản.
Marini cho biết: “Ở những người cao tuổi, bổ sung folate vào chế độ ăn có thể làm giảm tỉ lệ chất chuyển hóa nói trên đồng thời giảm nguy cơ mắc bệnh”.
Marini và Rine ước tính một người trung tuổi mang trong cơ thể 5 đột biến enzim hiếm gặp, mặc dù có lẽ không phải hiếm cho lắm, nhưng tình trạng vẫn có thể được cải thiện nhờ bổ sung vitamin và khoáng chất. “Có trên 600 loại enzim trong cơ thể người sử dụng vitamin và khoáng chất với vai trò cơ chất. Nghiên cứu này chỉ đưa ra những gì chúng tôi phát hiện được khi nghiên cứu một enzim trong số đó. Điều này có nghĩa là ngay cả khi tỉ lệ một người có khiếm khuyết xảy ra trên 1 gen là thấp, nhưng với 600 gen tất cả chúng ta đều có thể gặp đột biến tác động xấu đến chức năng của một hay nhiều enzim trong cơ thể”.
Ảnh hưởng khó phát hiện của biến thể enzim có thể giải thích kết quả không tương hợp của một số thử nghiệm y học, trong đó bao gồm dữ liệu không nhất quán về tác động của việc bổ sung vitamin. Trong tương lai, hồ sơ enzim của các đối tượng nghiên cứu sẽ được tính đến khi phân tích hiệu quả của thử nghiệm y học.
Trong bài viết, các nhà nghiên cứu có nêu: nếu chúng ta không chỉ tính đến enzim phụ thuộc vitamin mà tính đến 30.000 protein trong hệ gen của con người, “mỗi cá nhân sẽ có khoảng 250 biến thể thay thế có hại trong khi hiện tượng chỉ xảy ra với tần số thấp. Con số này cho thấy tác động tổng hợp của các biến thể tần số thấp cũng gây ra ảnh hưởng sinh lý to lớn”.
Thêm một lý do khuyến khích chúng ta tìm hiểu về hệ gen của chính bản thân mình. Rine cho biết: “Nếu chúng ta không đưa ra một lý do thuyết phục nào để mọi người quan tâm đến hệ gen của họ, và để hài lòng với thông tin di truyền cá nhân, thì lợi ích mà các nghiên cứu y sinh mang lại tùy theo đặc điểm di truyền nhất định cho đa số mọi người sẽ không bị bó hẹp trong khung thời gian. Động cơ của tôi một phần chính là khoa học, phần khác là dự án giáo dục, phần nữa là dự án chính trị”.
Marini cùng Rine đồng tình với nghiên cứu của Bruce Ames đã khuyến khích hai ông thực hiện tìm kiếm biến thể gen. Bruce Ames là giáo sư đã nghỉ hưu thuộc đại học California Berkeley ngành sinh học phân tử và tế bào, hiện ông thuộc nhóm nghiên cứu tại Viện nghiên cứu bệnh viện nhi Oakland. Vào thời điểm những năm 1970, Ames nhận thấy rất nhiều vi khuẩn trước đó không thể sản xuất một loại amino axit nhất định lại có thể thực hiện chức năng khi được cung cấp vitamin B6. Những năm gần đây, ông tiếp tục khám phá mối liên hệ giữa vi chất dinh dưỡng (micronutrient) và sức khỏe.
Rine nói: “Bruce nhận thấy có thể chữa bệnh di truyền ở vi khuẩn nhờ vitamin.” Do hệ gen của con người chứa khoảng 6 tỉ cặp bazơ trên ADN, mỗi một cặp đều có thể xảy ra đột biến nên tồn tại tới 3 đến 6 triệu điểm khác biệt về trình tự AND giữa hai người bất kì. Đưa ra con số này, ông giải thích, giống như vi khuẩn “con người cũng có nhu cầu về số lượng enzim khác nhau xét theo khía cạnh di truyền để enzim của họ đạt được hiệu quả tối đa”.
Vấn đề trên, theo Rine, có liên quan đến một trong những câu hỏi y sinh lớn đặt ra ngày nay. “Hiện chúng ta đã có trình tự gen hoàn thiện của các sinh vật mẫu phổ biến, trong đó có con người. Hiển nhiên là thử thách sinh học đặt ra trong thế kỉ 21 không phải là việc nhận diện gen mà là biến thể gen”.
Rine, Marini cùng cộng sự vẫn tiếp tục nghiên cứu biến thể trên gen MTHFR của con người cũng như các enzim sử dụng folate khác, đặc biệt quan tâm đến mối liên hệ giữa khiếm khuyết của những enzim này với dị tật bẩm sinh. Nhờ có số lượng sinh viên đông đảo – 1500 sinh viên – đang học tập tại phòng thí nghiệm sinh học 1A của ông, Rine có lợi thế trong việc tìm hiểu biến thể của enzim phụ thuộc vitamin B6 thứ hai có tên cystathionine beta-synthase.
Ông cũng tìm hiểu cơ chất enzim như vitamin và khoáng chất khôi phục enzim khiếm khuyết như thế nào. Ông ngờ rằng vitamin và khoáng chất bổ sung có vai trò làm chất đi kèm nhằm ổn định quy trình gấp nếp cấu trúc của enzim vốn là yếu tố then chốt đối với họat động xúc tác của enzim. “Đây là một nguyên tắc mới có thể được ứng dụng trong sản xuất dược phẩm”.
Đồng tác giả của nghiên cứu, ngoài Rine và Marini, còn có trợ lý nghiên cứu Jennifer Gin và Janet Ziegle thuộc đại học California Berkeley, Kathryn Hunkapiller Keho, David Ginzinger và Dennis A. Gilbert thuộc Cơ quan hệ thống sinh học ứng dụng. Cơ quan này cũng tài trợ một phần cho nghiên cứu. Ngoài ra nghiên cứu cũng được Quỹ tài trợ khám phá đại học California, DARPA và Viện y tế quốc gia tài trợ.

Thực vật kỳ dị sau thảm họa Fukushima
Thảm họa rò rỉ phóng xạ tại nhà máy điện hạt nhân Fukushima của Nhật cách đây 2 năm dường như đã gây ra những hậu quả lâu lâu dài và một trong số đó là khiến thực vật trong vùng ảnh hưởng bị đột biến dị thường.

Cận cảnh loại bướm có tên trong sách đỏ Việt Nam
Theo “Sách đỏ Việt Nam”, bướm khế có tên khoa học là Attacus atlas, cấp độ đe dọa xếp vào mức R (Rare: Hiếm, có thể sẽ nguy cấp). Loài bướm này được ghi nhận có kích thước lớn nhất ở nước ta và trên thế giới.

Độc đáo loài xương rồng tự chết để tiếp tục tồn tại và lan rộng khắp sa mạc
Không giống các loại xương rồng khác trên thế giới thường phát triển theo chiều dọc, Creeping Devil phát triển theo chiều ngang và nằm trên mặt đất.

15 loại trái cây được bình chọn ngon nhất thế giới
Chôm chôm, măng cụt, sầu riêng... là những loại trái cây được liệt vào danh sách quý hiếm và ngon nhất thế giới.

Loài sâu róm độc nhất thế giới
Trong các khu rừng nhiệt đới miền Nam Brazil có một loài sâu róm được người dân địa phương gọi là “chú hề lười biếng”, tên khoa học là Lonomia.

Ngắm nghía loài cây "quái vật nước dãi" xanh lè
Trên dãy núi Andes hàng nghìn tuổi tồn tại một loài thực vật có bề ngoài kì lạ đến mức mà có thể khiến chúng ta nhầm tưởng rằng chúng không thuộc về Trái đất này.



